La enfermedad suele diagnosticarse en etapas avanzadas, por ello, el cáncer de páncreas se ha convertido en la tercera causa principal de muerte por cáncer.
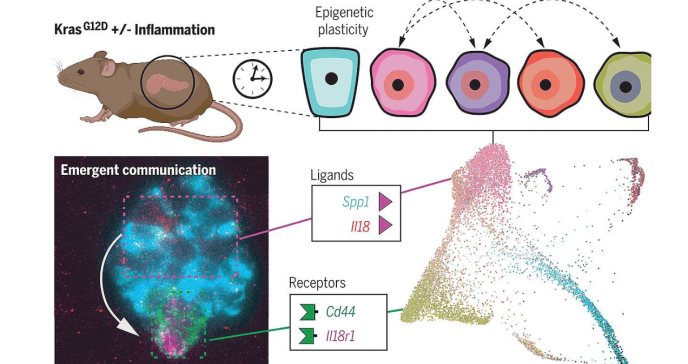
Las células que tienen estados epigenéticos aberrantes y pueden formar tumores tienen la capacidad de comunicarse de manera más efectiva con las células de su entorno. Un reciente estudio en ratones ha revelado cómo estos procesos afectan la plasticidad celular, que desempeña un papel fundamental en el inicio del cáncer de páncreas. Estos hallazgos abren nuevas posibilidades para el desarrollo de enfoques terapéuticos innovadores.
Mutaciones de ADN como precursoras de cáncer
Las mutaciones en el ADN son conocidas y estudiadas como causas del cáncer. Entre ellas, las mutaciones en el oncogén KRAS son frecuentes en el cáncer de pulmón, colorrectal y páncreas. Sin embargo, estas mutaciones sólo explican parcialmente el desarrollo de la enfermedad.
Recientemente, un estudio publicado en la revista Science por investigadores del Centro Oncológico Memorial Sloan Kettering (MSKCC) en Nueva York y Direna Alonso-Curbelo del Instituto de Investigación Biomédica (IRB Barcelona) ha revelado que las interacciones entre las mutaciones genéticas y factores externos, como una lesión tisular que provoque inflamación, pueden modificar la identidad de las células y su entorno local, lo que favorece la aparición y progresión de los tumores.
Cambios de las células en el cáncer de páncreas
En el cáncer de páncreas, se ha observado que los cambios en las células ocurren rápidamente, en un lapso de 24 a 48 horas después de una lesión tisular, de manera predecible. Esto conlleva un notable aumento en la capacidad de las células con mutación en KRAS para comunicarse e interactuar con otras células del entorno.
Para investigar estos procesos, se emplearon modelos de ratón genéticamente modificados y métodos computacionales avanzados, lo que permitió mapear los distintos estados celulares involucrados en el desarrollo del adenocarcinoma ductal pancreático (PDAC), el tipo más común de cáncer de páncreas.
¿Cómo la plasticidad celular impulsa el cáncer?
La plasticidad es la capacidad de las células para cambiar su identidad original y adaptarse a nuevas condiciones. En el contexto de la investigación, se ha descubierto que la inflamación aumenta esta plasticidad celular.
"Estas células precancerosas adquieren la capacidad de enviar y recibir muchas más señales que una célula normal", explicó la bióloga computacional Dana Pe'er, del MSKCC y coautora principal del estudio. "Vimos que esto no es aleatorio: está estructurado. Se observan los mismos patrones una y otra vez cuando se realizan los experimentos en diferentes ratones", añadió.
El estudio fue llevado a cabo por Cassandra Burdziak, estudiante de doctorado en el laboratorio de Pe'er, y Direna Alonso-Curbelo, quien previamente investigó en el laboratorio del coautor principal Scott Lowe en el MSKCC y ahora dirige su propio laboratorio en el IRB Barcelona.
Orígenes de la plasticidad
Para investigar los orígenes y los efectos de la plasticidad en las células con mutaciones en Kras, los científicos realizaron análisis de células individuales en tejidos normales, inflamados, premalignos y malignos utilizando modelos de ratones genéticamente modificados que reproducen con precisión muchos aspectos del cáncer de páncreas en humanos, desde su inicio hasta la metástasis.
"Estos modelos nos permitieron captar los cambios más tempranos en las células epiteliales pancreáticas a medida que se reprograman de un estado sano a un estado maligno", manifestó Lowe. Gracias al uso de análisis unicelulares, los investigadores pudieron descubrir las características de las subpoblaciones de células individuales presentes en cada etapa de la progresión del cáncer de páncreas, así como comprender cómo sus interacciones mutuas impulsan aún más dicho proceso.
Los investigadores diseñaron un nuevo método para medir la plasticidad celular
El equipo desarrolló un novedoso método para medir la plasticidad celular, que les permitió evaluar y cuantificar este fenómeno de manera precisa. Además, descubrieron que un aumento en la plasticidad celular se asociaba con la activación de genes relacionados con la comunicación entre células, incluyendo aquellos que codifican ligandos y receptores involucrados en esta interacción.
"Las células que muestran una mayor plasticidad en respuesta al oncogén KRAS y al daño tisular expresan genes que les permiten enviar y recibir señales específicas de su entorno, así como comunicarse con otras células", explica Pe'er. "Esto les confiere la capacidad de responder a señales que una célula normal no podría detectar. Además, estas células tienen una mayor capacidad de interactuar con las células del sistema inmunitario, lo que resulta en cambios en el sistema inmunológico que las rodea".
Adicionalmente, los investigadores identificaron que algunas subpoblaciones de células, incluyendo algunas muy poco frecuentes, desempeñan un papel fundamental como centros de comunicación, impulsando un bucle de retroalimentación que promueve el desarrollo y la progresión del cáncer de páncreas.
Se podría hallar el cáncer de páncreas en etapas tempranas
A través de experimentos adicionales, el equipo logró demostrar que estas interacciones celulares impulsan el desarrollo del cáncer. "Desarrollamos nuevos modelos genéticos para bloquear específicamente la señalización célula a célula asociada con la plasticidad neoplásica", destaca Alonso-Curbelo. "Estos análisis revelaron que estas amplias redes de comunicación que se establecen en las etapas iniciales del cáncer de páncreas son funcionalmente relevantes y juegan un papel crucial en la tumorigénesis pancreática en ratones".
En resumen, esta investigación brinda una nueva perspectiva detallada sobre cómo las células que portan una copia mutada del gen KRAS adquieren plasticidad y promueven la progresión del cáncer en presencia de inflamación.
"Esto nos proporciona una nueva guía que puede ayudar en el desarrollo de estrategias para la detección o incluso prevención de tumores pancreáticos antes de que alcancen etapas avanzadas", afirma Lowe. "Comprender cómo las redes de comunicación entre células impulsan el inicio del cáncer de páncreas ofrece prometedoras posibilidades para el desarrollo de terapias que bloqueen o ralenticen la progresión temprana del cáncer, e incluso para la enfermedad en fases más avanzadas".
Fuente consultada aquí.