En el estudio, los pacientes que recibieron dosis de este medicamento mostraron una importante mejoría en comparación con el grupo de placebo.
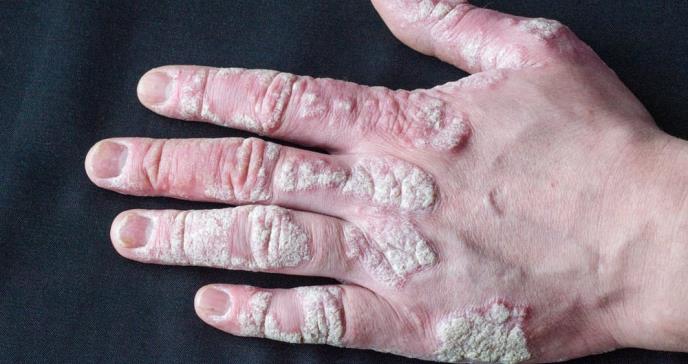
El brepocitinib ha demostrado una notable mejora en la reducción de los síntomas en adultos que padecen artritis psoriásica activa moderada o grave, en comparación con un grupo de control que recibió placebo.
Este fármaco tiene una combinación de inhibidores de la tirosina cinasa 2 y la cinasa Janus 1 (JAK), está siendo objeto de estudio para el tratamiento de diversas enfermedades de origen inmunológico, incluyendo la artritis psoriásica.
Esta investigación ha sido conducida por el Dr. Philip Mease, quien se desempeña en el Swedish Medical Center de Providence St. Joseph Health y en la University of Washington, ambas instituciones ubicadas en Seattle, Estados Unidos.
Eficacia y mecanismo de actuación del brepocitinib
La eficacia de los inhibidores de la cinasa Janus y los inhibidores de la tirosina cinasa 2 en pacientes con artritis psoriásica ha sido respaldada previamente por estudios, aunque se ha enfatizado la necesidad de recabar más datos en pacientes con artritis psoriásica activa.
Este beneficio se mantuvo constante tanto a las 16 semanas como al año de seguimiento, según se desprende de datos obtenidos de un grupo de 218 individuos participantes en un ensayo de fase 2b.
Desarrollo del estudio en pacientes con artritis psoriásica
En un estudio publicado en la revista "Arthritis & Rheumatology", se llevó a cabo una asignación aleatoria de adultos con edades comprendidas entre los 18 y los 75 años que padecían artritis psoriásica moderada o grave. Estos individuos recibieron dosis orales diarias de brepocitinib en tres variantes: 10 mg, 30 mg o 60 mg, o bien, se les administró un placebo durante 16 semanas.
Esta fase del estudio tenía como objetivo evaluar la tolerabilidad, la eficacia y la respuesta a diferentes dosis [1]. Los pacientes que habían recibido el placebo fueron cambiados a dosis de 30 mg o 60 mg de brepocitinib en la semana 16.
Los datos iniciales de los participantes y las características de la enfermedad se mantuvieron en equilibrio entre los distintos grupos de tratamiento. Las puntuaciones medias para la Puntuación de Actividad de la Enfermedad Artrítica Psoriásica (PASDAS) y el Índice de Actividad de la Enfermedad para la artritis psoriásica fueron de 5,6 y 38,2, respectivamente, en la población general del estudio.
Además, aproximadamente dos tercios (64,7%) de los participantes presentaban una puntuación inicial del Índice de Área y Gravedad de la Psoriasis (PASI) superior a 0 y un 3% o más de superficie corporal afectada por la psoriasis.
Criterios importantes en el estudio del brepocitinib
El criterio principal de valoración consistió en la proporción de pacientes que lograron una mejora del 20% en los criterios de respuesta establecidos por el American College of Rheumatology (ACR 20) a las 16 semanas. Entre tanto, los criterios secundarios abordaron las tasas de pacientes que cumplieron los criterios de respuesta en un 50% (ACR 50) y un 70% (ACR 70), la proporción de pacientes que lograron una mejora del 75% y del 90% en las puntuaciones del Índice de Área y Gravedad de la Psoriasis (PASI 70 y PASI 90), así como las tasas de pacientes que cumplieron los criterios de actividad mínima de la enfermedad (MDA) a las 16 y 52 semanas.
Resultados prometedores para los pacientes
Los resultados revelaron que en la semana 16, las tasas de respuesta ACR 20 fueron significativamente mayores en los grupos que habían recibido brepocitinib en dosis de 30 mg y 60 mg, en comparación con el grupo que recibió placebo (66,7% y 74,6%, respectivamente, frente al 43,3%), aunque no se observaron diferencias significativas en el grupo que había recibido brepocitinib en dosis de 10 mg (64,5%).
Las tasas de respuesta para ACR 50, ACR 70, PASI 75, PASI 90 y actividad mínima de la enfermedad fueron igualmente superiores en los grupos tratados con 30 mg y 60 mg de brepocitinib, en comparación con el grupo de placebo, y estas respuestas se mantuvieron consistentes a lo largo de la semana 52. Cabe destacar que se observaron diferencias significativas en las tasas de respuesta PASI 75 y PASI 90 para los pacientes que habían recibido 30 mg y 60 mg de brepocitinib, en comparación con el grupo de placebo, incluso desde las semanas 4 y 8, respectivamente.
Adicionalmente, la actividad de la enfermedad, evaluada mediante la Puntuación de Actividad de la Enfermedad Artrítica Psoriásica (PASDAS), mostró una mejora significativa desde el inicio hasta la semana 16 en todos los grupos tratados con brepocitinib, en comparación con aquellos que recibieron placebo.
En cuanto a la tolerabilidad, los investigadores informaron que los datos generales concordaban con estudios previos sobre brepocitinib, y que la mayoría de los efectos adversos experimentados fueron de carácter leve o moderado. En total, 12 participantes (5,5%) reportaron un total de 15 efectos adversos graves, incluyendo 6 infecciones entre aquellos que habían recibido dosis de 30 mg o 60 mg de brepocitinib. Es relevante señalar que no se registraron eventos adversos cardiovasculares graves ni fallecimientos durante el período del estudio.
Limitaciones que presentó la investigación
No obstante, los hallazgos del estudio presentan ciertas limitaciones, como el uso de clínicas en una región geográfica limitada (11 países de Europa), el tamaño reducido de la muestra y la predominancia de participantes de origen étnico caucásico, según lo señalaron los investigadores. Otras limitaciones notables incluyen el efecto placebo significativo y el período relativamente breve de control con placebo.
Este estudio contó con el respaldo de Pfizer. El Dr. Mease declaró tener relaciones financieras con Pfizer y otras compañías como AbbVie, Amgen, Bristol-Myers Squibb, Boehringer Ingelheim, Galapagos, Gilead, GlaxoSmithKline, Inmagene, Janssen, Lilly, Novartis, Sun y UCB. Además, varios coautores eran empleados de Pfizer, y otros declararon tener relaciones económicas con Pfizer y otras empresas farmacéuticas.
Fuente consultada aquí